- Pengarang Jason Gerald gerald@how-what-advice.com.
- Public 2023-12-16 11:29.
- Diubah suai terakhir 2025-01-23 12:42.
Pengenceran adalah proses menjadikan larutan pekat lebih cair. Terdapat pelbagai alasan mengapa seseorang mungkin ingin melakukan pencairan, mulai dari alasan yang serius hingga yang sederhana. Sebagai contoh, ahli biokimia mencairkan larutan dari bentuk pekatnya untuk membuat penyelesaian baru untuk digunakan dalam eksperimen, sedangkan, sebaliknya, bartender sering mencairkan minuman keras dengan minuman ringan atau jus untuk menjadikan koktel lebih enak. Formula umum untuk mengira pencairan adalah C1V1 = C2V2, dengan C1 dan C2 mewakili kepekatan awal dan akhir larutan, dan V1 dan V2 mewakili isipadu.
Langkah
Kaedah 1 dari 2: Mencairkan Pekat dengan tepat melalui Persamaan Pencairan

Langkah 1. Tentukan apa yang anda tahu dan tidak tahu
Pengenceran dalam kimia biasanya bermaksud mengambil sebilangan kecil larutan yang anda tahu kepekatannya, kemudian menambahkan cecair neutral (seperti air) untuk membuat larutan baru dengan isipadu yang lebih besar tetapi kepekatan yang lebih rendah. Ini sangat sering dilakukan di makmal kimia, kerana, demi keberkesanannya, reagen sering disimpan dalam kepekatan yang sangat tinggi, yang kemudian dicairkan untuk digunakan dalam eksperimen. Biasanya, dalam kebanyakan situasi dunia nyata, anda akan mengetahui kepekatan penyelesaian awal anda dan kepekatan atau isi padu yang anda mahukan kepekatan akhir anda, tetapi bukan jumlah penyelesaian awal yang anda perlukan untuk mendapatkan penyelesaian akhir.
- Walau bagaimanapun, dalam situasi lain (terutama dalam masalah sekolah), anda mungkin perlu mencari potongan teka-teki lain - contohnya, anda mungkin diberi jumlah dan kepekatan awal, kemudian diminta untuk mencari kepekatan terakhir jika anda mencairkan penyelesaiannya. ke isipadu yang dikehendaki. Dalam keadaan pencairan, ada baiknya perhatikan pemboleh ubah yang diketahui dan tidak diketahui sebelum memulakan.
-
Mari kita selesaikan contoh soalan. Katakan kita diminta mencairkan larutan 5 M dengan air untuk membuat 1 L larutan 1. mM. Dalam kes ini, kita mengetahui kepekatan larutan awal kita dan jumlah dan kepekatan akhir yang kita mahukan, tetapi bukan jumlah larutan awal yang perlu kita tambahkan dengan air untuk mencapai hasil yang diinginkan.
Peringatan: Dalam kimia, M adalah pengukuran kepekatan yang disebut Molarity, yang menunjukkan mol suatu bahan per liter
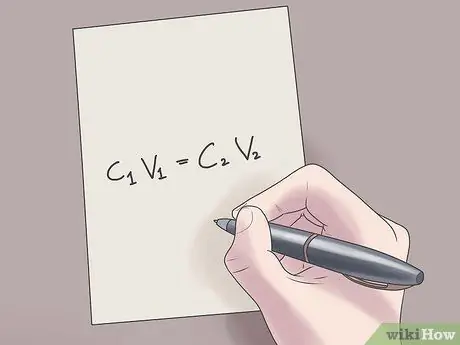
Langkah 2. Masukkan nilai anda ke dalam formula C1V1 = C2V2.
Dalam formula ini, C1 ialah kepekatan awal larutan, V1 ialah isipadu penyelesaian awal, C2 adalah kepekatan akhir larutan, dan V2 adalah isipadu penyelesaian terakhir. Memasukkan nilai yang diketahui ke dalam persamaan ini akan membantu anda mencari nilai yang tidak diketahui dengan lebih sukar.
- Anda mungkin berguna untuk meletakkan tanda tanya di hadapan unit yang ingin anda cari untuk membantu anda menyelesaikannya.
-
Mari kita teruskan contoh kita. Kami akan memasukkan nilai yang kami ketahui seperti berikut:
- C1V1 = C2V2
- (5 M) V1 = (1 mM) (1 L). Dua kepekatan kami mempunyai unit yang berbeza. Mari berhenti di sini dan terus ke langkah seterusnya.

Langkah 3. Pertimbangkan sebarang perbezaan unit
Oleh kerana penyelesaian melibatkan perubahan konsentrasi (yang kadangkala cukup besar), tidak mustahil kedua pemboleh ubah dalam persamaan anda mempunyai unit yang berbeza. Walaupun ini mudah dilupakan, unit yang tidak sama dalam persamaan anda boleh menyebabkan jawapan anda tidak betul. Sebelum selesai, ubah semua nilai dengan unit kepekatan dan / atau isipadu yang berbeza.
-
Dalam contoh kami, kami menggunakan unit yang berlainan untuk kepekatan M (molar) dan mM (milimolar). Mari ubah ukuran kedua kami ke M:
- 1 mM × 1 M / 1,000 mM
- = 0.001 M

Langkah 4. Selesaikan
Setelah semua unit sama, selesaikan persamaan anda. Ini hampir selalu dapat dilakukan dengan algebra sederhana.
-
Kami menghentikan masalah contoh kami di sini: (5 M) V1 = (1 mM) (1 L). Mari cari nilai V1 dengan unit baru kami.
- (5 M) V1 = (0.001 M) (1 L)
- V1 = (0.001 M) (1 L) / (5 M).
-
V1 = 0,0002 L, atau 0,2 mL.

Langkah 5. Fahami cara menggunakan jawapan anda dengan betul
Katakan anda telah menemui nilai yang hilang, tetapi anda tidak pasti bagaimana menggunakan maklumat baru ini dalam pencairan sebenar yang perlu anda lakukan. Ini dapat difahami - bahasa matematik dan sains kadang-kadang tidak sesuai dengan dunia nyata. Apabila anda mengetahui empat nilai dalam persamaan C1V1 = C2V2, lakukan pencairan seperti berikut:
- Ukur isipadu V1 dari larutan dengan kepekatan C1. Kemudian, tambahkan pengencer yang mencukupi (air, dll.) Untuk menjadikan jumlah isi keseluruhan V2. Penyelesaian baru ini akan mempunyai kepekatan yang anda mahukan (C2).
- Dalam contoh kami, sebagai contoh, pertama-tama kita mengukur 0.2 mL larutan 5 M. Seterusnya, kita akan menambahkan air yang cukup untuk meningkatkan isipadu larutan menjadi 1 L: 1 L - 0,0002 L = 0,9998 L, atau 999, 8 mL. Dengan kata lain, kita akan menambahkan 999.8 mL air ke dalam larutan sampel kecil kita. Larutan cair baru kami mempunyai kepekatan 1 mM, yang merupakan kepekatan yang kami mahukan.
Kaedah 2 dari 2: Membuat Penyelesaian Pencairan Mudah dan Praktikal

Langkah 1. Baca sebarang pembungkusan untuk maklumat
Terdapat pelbagai sebab mengapa anda mungkin ingin membuat penyelesaian pencairan di rumah, di dapur, atau di makmal bukan kimia lain. Contohnya, membuat jus oren dari pekat sederhana adalah pencairan. Dalam banyak kes, produk yang perlu dicairkan mengandungi maklumat mengenai pencairan yang perlu dibuat, di suatu tempat pada bungkusan. Mereka mungkin mempunyai arahan yang tepat untuk diikuti. Berikut adalah beberapa perkara yang perlu dicari ketika mencari maklumat:
- Jumlah produk yang digunakan
- Isipadu pelarut yang digunakan
- Jenis pelarut yang digunakan (biasanya air)
- Arahan pencampuran khas
- Anda mungkin tidak melihat maklumat mengenai kepekatan cecair yang digunakan. Maklumat ini tidak berguna untuk pengguna biasa.

Langkah 2. Tambahkan bahan yang berfungsi sebagai pelarut ke larutan pekat
Untuk pencairan isi rumah yang sederhana, seperti yang mungkin anda buat di dapur, anda hanya perlu mengetahui jumlah pekatan yang anda gunakan dan anggaran kepekatan akhir yang anda mahukan sebelum anda memulakannya. Cairkan pekat dengan jumlah pengencer yang sesuai, yang ditentukan bergantung pada isipadu pekat awal yang digunakan. Lihat di bawah:
- Sebagai contoh, jika kita mahu mencairkan 1 cawan pekat jus oren hingga 1/4 kepekatan awalnya, kita akan menambah 3 cawan air ke dalam pekat. Campuran terakhir kami akan mempunyai 1 cawan pekat dalam 4 cawan keseluruhan cecair - 1/4 kepekatan awalnya.
- Inilah contoh yang lebih rumit: Sekiranya kita ingin mencairkan 2/3 cawan pekat menjadi 1/4 kepekatan awalnya, kita akan menambah 2 cawan air, kerana 2/3 cawan sama dengan 1/4 kali 2 & 2/3 cawan cecair keseluruhan.
- Pastikan anda memasukkan bahan anda ke dalam bekas yang cukup besar untuk menyimpan jumlah akhir yang anda mahukan - mangkuk besar atau bekas serupa.

Langkah 3. Abaikan jumlah serbuk dalam kebanyakan kes
Menambah serbuk (seperti campuran minuman tertentu) ke dalam cecair biasanya tidak dianggap sebagai pencairan. Perubahan isipadu yang dihasilkan daripada penambahan sejumlah kecil serbuk ke cecair biasanya cukup kecil sehingga boleh diabaikan. Dengan kata lain, semasa menambahkan sebilangan kecil serbuk ke cecair, cukup masukkan serbuk ke isi padu akhir yang anda inginkan dan campurkan.
Amaran
- Ikuti sebarang garis panduan keselamatan yang diberikan oleh pengeluar atau yang dikehendaki oleh syarikat anda. Ini amat penting jika anda perlu mencairkan larutan asid.
- Mengusahakan penyelesaian berasid mungkin memerlukan langkah dan panduan keselamatan yang lebih terperinci daripada penyelesaian bukan berasid.






